Miért olyan nehéz az AI-t rákdiagnosztikára használni?
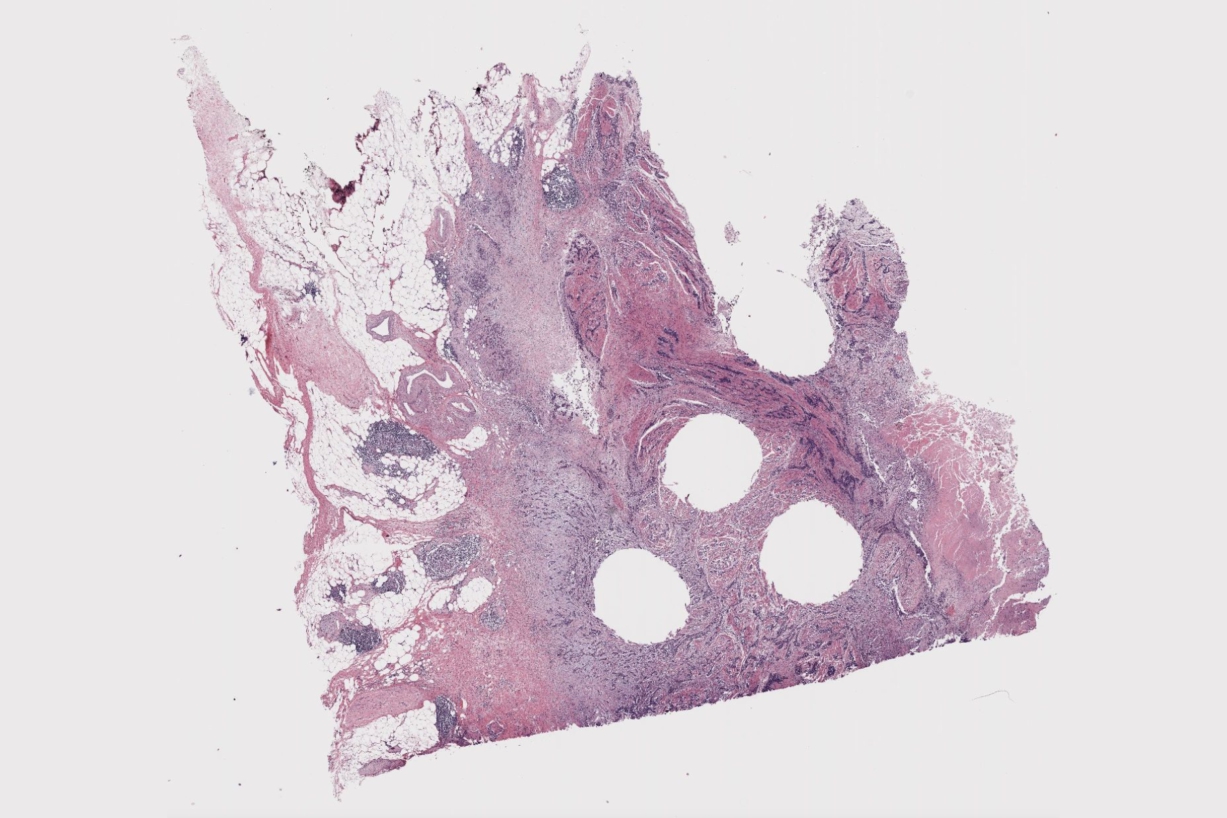
A test belsejének vizsgálata és a rák diagnosztizálása minta felismerésén alapul. A radiológusok röntgen és mágneses rezonancia készülékekkel világítják meg a daganatokat, míg a patológusok mikroszkóp alatt vizsgálják a vese, máj és más szöveteket, hogy felismerjék a rákra utaló mintákat. Ezek a minták megmutatják, milyen súlyos a rák, milyen kezelések lehetnek hatékonyak, és hol terjedhet tovább a daganat.
Az AI és a mintafelismerés
Elvileg a mesterséges intelligencia (AI) rendkívül hasznos lehetne ebben a folyamatban. Andrew Norgan, a Mayo Clinic digitális patológiai platformjának orvosi igazgatója szerint: „A mi munkánk a mintafelismerésről szól. Megnézzük a szövetmintákat, és információkat gyűjtünk, amelyek bizonyítottan fontosak.”
A vizuális elemzés egy olyan terület, ahol az AI az elmúlt 15 évben jelentős fejlődésen ment keresztül. Képzeljük el, hogy egy AI algoritmus valamikor képes lehet észrevenni valamit, amit egy emberi patológus esetleg elnézett, vagy legalábbis gyorsítani tudja a diagnosztikai folyamatot. Az utóbbi években sok új modell készült, de ezek még mindig kísérleti szakaszban vannak. Mitől lesz egy AI modell elég jó ahhoz, hogy a valós klinikai gyakorlatban használják?
Az Aignostics AI egészségügyi vállalat és a Mayo Clinic által vezetett, egy ilyen modell létrehozására irányuló legújabb erőfeszítés részleteit nemrégiben tették közzé az arXiv-on. A tanulmányt nem bírálták el, de sokat elárul arról, hogy milyen kihívásokkal jár egy ilyen eszköz valós klinikai környezetbe való átültetése.
Az Atlas modell
A Mayo Clinic és az AI-alapú egészségügyi cég, az Aignostics, nemrégiben bemutatott egy új modellt, az Atlast. Az Atlas együttesen 1,2 millió szövetmintán és 490 ezer eset adataiból tanult. Az AI modell pontosságát hat másik vezető AI patológiai modellel hasonlították össze. Az Atlas kilenc tesztből hat esetben felülmúlta riválisait. Különösen jó eredményt ért el a vastagbélrákos szövetek kategorizálásában, ahol 97,1%-ban megegyezett az emberi patológusok következtetéseivel. Ugyanakkor a prosztatarákos daganatok osztályozásában csupán 70,5%-os pontosságot ért el.
„Kilencven százalék valószínűleg nem elég jó. Még jobbnak kell lennie”, mondta Carlo Bifulco, a Providence Genomics orvosi igazgatója. Azonban hozzátette, hogy az ilyen modellek még nem tökéletes teljesítmény mellett is segíthetik a patológusok munkáját, gyorsabb diagnózisokat eredményezve.
Az adatok hiánya és a technikai akadályok
Az AI modellek teljesítményét elsősorban a tréningadatok mennyisége korlátozza. Andrew Norgan szerint az amerikai patológiai gyakorlatok kevesebb mint 10%-a digitalizált. Ez azt jelenti, hogy a szövetmintákat hagyományos módon mikroszkóppal elemzik, majd hatalmas nyilvántartásokban tárolják, anélkül hogy digitális formába kerülnének. Európában nagyobb mértékű digitalizáció tapasztalható, de még így is kevés az elérhető adat.
A Mayo Clinic 2022-ben előrelátta ezt a problémát, és átfogó digitalizálási projektet indított. Egy robot segítségével nagy felbontású fényképeket készítettek a szövetmintákról, havi egymillió mintát feldolgozva. Ezek az erőfeszítések biztosították az Atlas modellhez szükséges 1,2 millió magas minőségű szövetmintát.
Egy másik technikai probléma a szövetminták apró mérete és nagy felbontású digitalizálása. Ezek a képek gyakran több mint 14 milliárd pixelt tartalmaznak, ami hatalmas tárhelyigényt eredményez. Az AI modellek képzése során részleteket kell kiválasztani ezekből a képekből, ami újabb kihívásokat teremt.
Az Atlas modellt olyan teszteken is vizsgálták, amelyek molekuláris szinten kísérelték meg a daganatok elemzését. Ezek a tesztek megpróbálják megérteni, hogy mi történik a minták molekuláris szintjén, például a DNS hibák kijavításáért felelős mechanizmusokkal kapcsolatban. Az Atlas teljesítése átlagosan 44,9% volt ezeken a teszteken – a legjobb eredmény eddig, de még mindig messze elmarad az ideálistól.
Előrelépések és további kihívások
Carlo Bifulco szerint az Atlas modell valós előrelépést jelent, de nagyobb adatbázisokra és új modellstratégiákra lesz szükség ahhoz, hogy drámai fejlődés következzen be. Az AI rákdiagnosztikában való alkalmazásának legnagyobb akadályai jelenleg az adatok elérhetősége, a képzési módszerek optimalizálása és a molekuláris elemzések megbízhatósága. Mindezek ellenére a technológia fejlődése reményt keltő, és a közeljövőben segítheti a patológusok munkáját, gyorsabb és pontosabb diagnózisokat biztosítva. Az AI nemcsak az orvoslás, hanem a betegek életminõségének javításában is kulcsfontosságú szerepet tölthet be a jövőben.
Érdekelhet még:
- Humanoid robotok készülnek maratont futni Kínában
- A L’Oréal a mesterséges intelligencia segítségével újradefiniálja a kozmetikai ipart
- Az AI-nak köszönhetően nő a hamis letartóztatások száma?
- Úttörő technológia a rákos sejteket normál sejtekké alakítja át